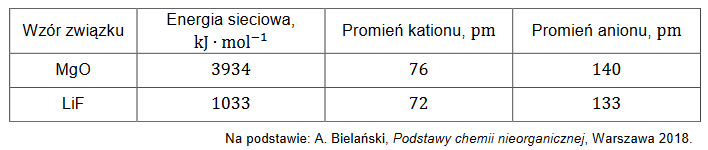
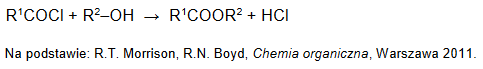Właściwości kwasu solnego
Arkusz z chemii rozszerzonej maj 2024 Formuła 2015
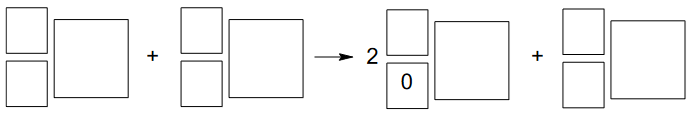
Reakcja kwasu solnego z wodorotlenkiem baru przebiega zgodnie z równaniem:
H3O+ + OH– → 2H2O
Oblicz, ile 𝐜𝐦𝟑 wodnego roztworu wodorotlenku baru o stężeniu molowym równym 𝟎, 𝟎𝟐𝟎 𝐦𝐨𝐥 ∙ 𝐝𝐦−𝟑 należy dodać do 𝟐𝟓 𝐜𝐦𝟑 kwasu solnego o pH = 1,5, aby otrzymany roztwór miał pH równe 3,7. Przyjmij, że objętość powstałego roztworu jest sumą objętości użytych roztworów.
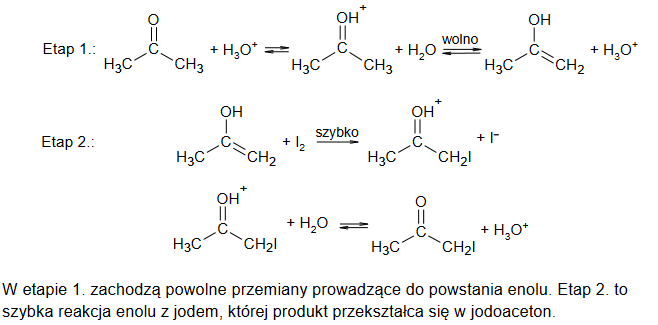
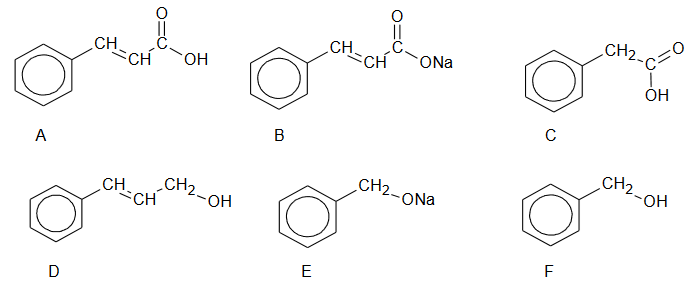
ciąg przemian związków organicznych
Arkusz z chemii rozszerzonej maj 2024 Formuła 2015
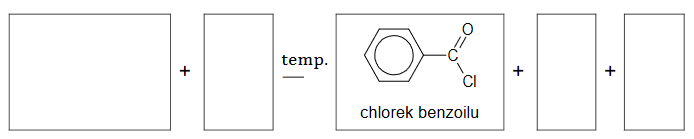
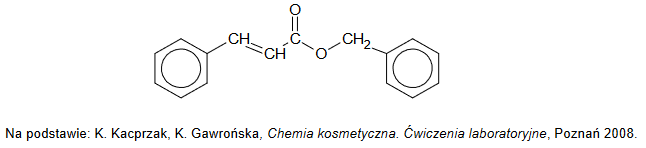
Na poniższym schemacie przedstawiono ciąg przemian związków organicznych A, B i C:
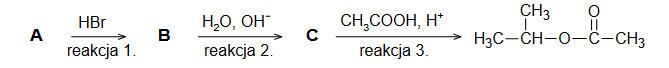
1. Napisz wzory półstrukturalne (grupowe) związków oznaczonych na schemacie literami A, B i C.
2. Określ typ reakcji (addycja, eliminacja, substytucja) oraz mechanizm (elektrofilowy, nukleofilowy, rodnikowy) reakcji oznaczonych na schemacie numerami 1. i 2.

Liczba koordynacyjna
Arkusz z chemii rozszerzonej maj 2024 Formuła 2023
Liczba koordynacyjna to liczba najbliższych atomów lub jonów otaczających dany atom lub jon w sieci krystalicznej kryształu.
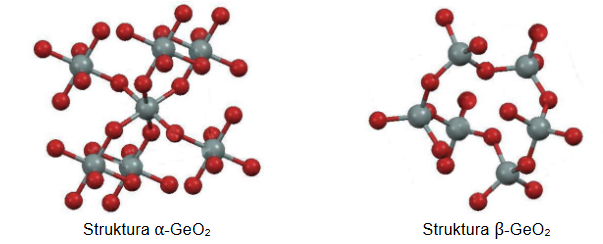
Tlenek germanu(IV) jest krystalicznym ciałem stałym. Istnieje w dwóch odmianach: alfa, α-GeO2, oraz beta, β-GeO2. Fragmenty struktur obu odmian przedstawiono poniżej (atomy Ge – szare, atomy O – czerwone).
Uzupełnij zdania. Wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie.
W odmianie α-GeO2 liczba koordynacyjna dla atomu germanu wynosi (dwa / cztery / sześć). W strukturze odmiany β-GeO2 dla orbitali walencyjnych atomu germanu zakłada się hybrydyzację (sp2 / sp3).
stężenia kationów srebra(I)
Arkusz z chemii rozszerzonej maj 2024 Formuła 2023
Zmieszano równe objętości dwóch wodnych roztworów: azotanu(V) srebra(I) o stężeniu c1 = 1 ∙ 10−4 mol ∙ dm−3 i chlorku potasu o stężeniu c2 = 2 ∙ 10−6 mol ∙ dm−3. Podczas doświadczenia utrzymywano temperaturę równą 25 °C.
Uzupełnij poniższe zdania. Wpisz wartość iloczynu stężeń kationów srebra(I) i anionów chlorkowych po zmieszaniu roztworów oraz wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie.
Iloczyn stężeń kationów srebra(I) i anionów chlorkowych w otrzymanej mieszaninie jest równy ….. . Jego wartość jest (mniejsza / większa) od wartości iloczynu rozpuszczalności chlorku srebra(I), dlatego osad tej soli się (nie wytrąci / wytrąci).
odczyn wodnych roztworów trzech soli
Arkusz z chemii rozszerzonej maj 2024 Formuła 2023
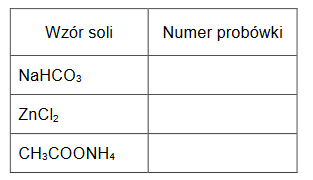
Zbadano odczyn wodnych roztworów trzech soli: NaHCO3, ZnCl2 i CH3COONH4 za pomocą uniwersalnych papierków wskaźnikowych. Wyniki doświadczenia pokazano na zdjęciu.

1. Uzupełnij tabelę. Przyporządkuj numery probówek do wzorów badanych soli.
2. Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, albo F – jeśli jest fałszywe.

reakcje z wodnym roztworem chlorku manganu(II)
Arkusz z chemii rozszerzonej maj 2024 Formuła 2023
W 150 cm3 wodnego roztworu chlorku manganu(II) o stężeniu molowym 𝑐 = 0,678 mol ∙ dm−3 i gęstości 𝑑 = 1,07 g ∙ cm−3 rozpuszczono 6,00 g hydratu tej soli o wzorze MnCl2 ∙ 4H2O.
Na podstawie: Z. Dobkowska, K.M. Pazdro, Szkolny poradnik chemiczny, Warszawa 2020.
Oblicz, jaki procent masy otrzymanego roztworu stanowi masa chlorku manganu(II). Załóż, że objętość roztworu się nie zmieniła. Przyjmij wartości mas molowych: MMnCl2 = 126 g ∙ mol–1 oraz MMnCl2 ∙ 4H2O = 198 g ∙ mol–1.
Chemia nieorganiczna
Arkusz z chemii rozszerzonej maj 2024 Formuła 2023
Jony FeO4 2– mogą powstać podczas reakcji Fe(OH)3 z jonami ClO– w nasyconym roztworze NaOH, zilustrowanej poniższym schematem:
Fe(OH)3 + ClO– + OH– → FeO42– + Cl– + H2O
Na podstawie: L. Kolditz, Chemia nieorganiczna, Warszawa 1994.
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania zachodzącej podczas opisanej przemiany. Uwzględnij środowisko reakcji. Uzupełnij
współczynniki stechiometryczne w poniższym schemacie.
Równanie reakcji utleniania:
…… Fe(OH)3 + …… ClO– + …… OH– → …… FeO42– + …… Cl– + …… H2O
Reakcje w półogniwach redoks
Arkusz z chemii rozszerzonej maj 2024 Formuła 2023
Poniżej przedstawiono równania reakcji, które przebiegają w wybranych półogniwach redoks.

W tych półogniwach elementem przewodzącym jest platyna – nie bierze ona udziału w reakcji elektrodowej.
1. Uzupełnij poniższy zapis, tak aby powstał schemat ogniwa galwanicznego zbudowanego z półogniw A i B, które generuje prąd w warunkach standardowych. Napisz, które półogniwo pełni funkcję anody, a które – katody w pracującym ogniwie.
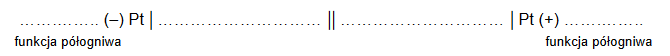
2. Napisz w formie jonowej sumaryczne równanie reakcji, która zachodzi w pracującym ogniwie zbudowanym z półogniw A i B.
Stężeniowa stała równowagi
Arkusz z chemii rozszerzonej maj 2024 Formuła 2023
Stężeniowa stała równowagi reakcji zilustrowanej poniższym równaniem:
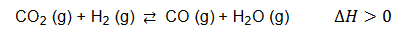
w temperaturze T wynosi 1,0.
1. Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, albo F – jeśli jest fałszywe.

2. W reaktorze o pojemności 1,0 dm3 zmieszano w temperaturze T tlenek węgla(IV) i wodór. Sumaryczna liczba moli tych reagentów była równa 10.
Oblicz początkową liczbę moli tlenku węgla(IV) i początkową liczbę moli wodoru w mieszaninie, jeżeli wiadomo, że do momentu ustalenia się stanu równowagi w temperaturze T przereagowało 60 % wodoru.