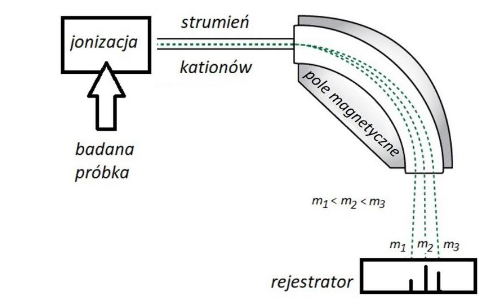
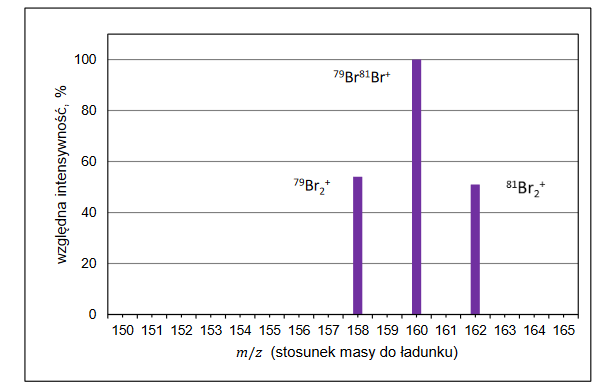
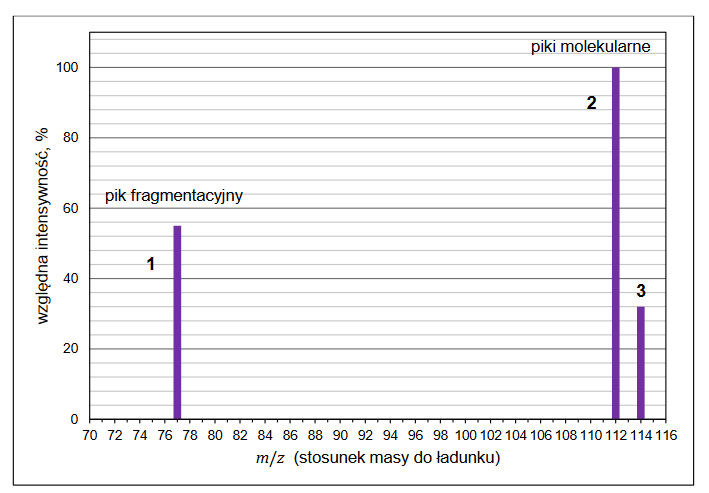
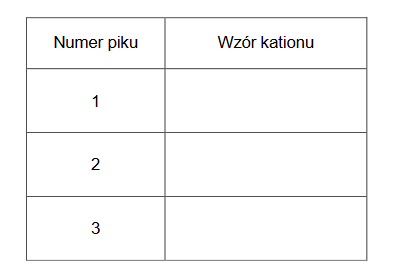
kinetyka reakcji utleniania jonów bromkowych jonami bromianowymi(V)
Arkusz diagnostyczny z chemii 2022 grudzień
Badano kinetykę reakcji utleniania jonów bromkowych jonami bromianowymi(V) w środowisku kwasowym, która przebiega zgodnie z równaniem:
5Br⁻ + BrO₃⁻ + 6H+ → 3Br₂ + 3H₂O
Na podstawie pomiarów kinetycznych ustalono następującą zależność między szybkością tej
reakcji a stężeniami reagentów:
𝑣 = 𝑘 ⸱ [Br⁻] ⸱ [BrO₃⁻] ⸱ [H+]₂
1. Stała szybkości reakcji w zależności od postaci równania kinetycznego może mieć różny wymiar. Niżej przedstawiono przykładowe wyrażenia oznaczone literami A–D.
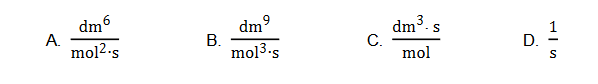
Uzupełnij poniższe zdania. Wybierz i zaznacz jedną odpowiedź spośród podanych
w każdym nawiasie.
Stała szybkości reakcji utleniania jonów bromkowych jonami bromianowymi(V) ma jednostkę oznaczoną literą (A / B / C / D). Jedno z podanych wyrażeń nie może być jednostką stałej szybkości reakcji. To wyrażenie oznaczono literą (A / B / C / D).
2. Oblicz, jak zmieni się szybkość opisanej reakcji, jeżeli początkowe pH roztworu będzie wyższe o 𝟎, 𝟑.
gęstości wody bromowej i chloroformu
Arkusz diagnostyczny z chemii 2022 grudzień
Na zdjęciu obok pokazano dwuetapowe doświadczenie, podczas którego do probówki wprowadzono kilka cm³ chloroformu (CHCl₃) oraz wodę bromową (etap 1.), a następnie ciecze wymieszano i pozostawiono na pewien czas (etap 2.).

Przedstaw wniosek z pokazanego doświadczenia dotyczący porównania gęstości wody bromowej i chloroformu. Nazwij proces, który spowodował zmianę wyglądu zawartości probówki po wymieszaniu i ponownym rozdzieleniu się cieczy.
Gęstość chloroformu jest ? niż gęstość wody bromowej.
Nazwa procesu:
metody wykrywania obecności jonów bromkowych
Arkusz diagnostyczny z chemii 2022 grudzień
Jedna z metod wykrywania obecności jonów bromkowych albo jodkowych w roztworze polega na utlenieniu ich do wolnego bromu albo jodu.
Rozstrzygnij, czy zarówno jony bromkowe, jak i jony jodkowe można utlenić za pomocą kwasu azotowego(V). Uzasadnij swoją odpowiedź. W uzasadnieniu odnieś się do wartości odpowiednich potencjałów standardowych.
Rozstrzygnięcie:
– jony bromkowe:
– jony jodkowe:
Uzasadnienie:
Elektrochemia – Ogniwa
Arkusz diagnostyczny z chemii 2022 grudzień
Zbudowano dwa ogniwa składające się z półogniw metalicznych (I rodzaju). W jednym z ogniw półogniwo cynkowe stanowi anodę, a w drugim – katodę. Wartości SEM tych ogniw różnią się o 59 mV.
Uzupełnij schematy opisanych ogniw.
Elektrodą w dobieranym półogniwie powinien być jeden z wymienionych metali:
mangan chrom żelazo kobalt miedź
Schematy ogniw:
A ( ̶ ): Zn │ Zn2+║ ………. │ ………. :(+) K
A ( ̶ ): …….… │ ………. ║ Zn2+ │ Zn :(+) K
procesy polimeryzacji i kondensacji
Arkusz diagnostyczny z chemii 2022 grudzień
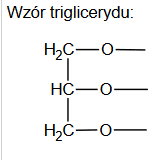
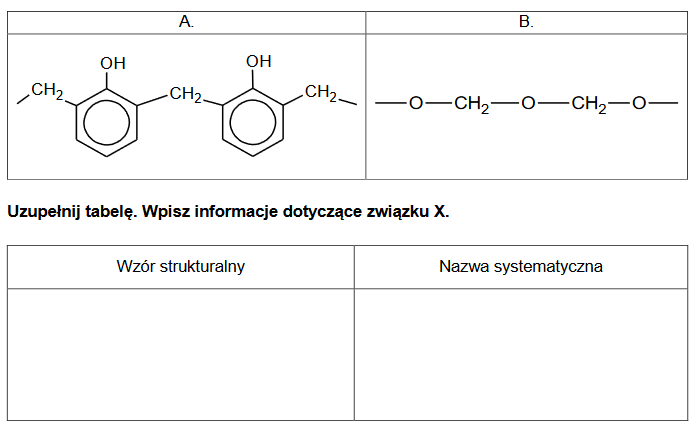
Związek organiczny X jest substratem w procesach produkcji niektórych tworzyw sztucznych. Ten związek ulega reakcji polimeryzacji i jest stosowany jako jeden z reagentów w procesach polikondensacji. Niżej przedstawione są wzory fragmentów łańcucha dwóch polimerów (oznaczonych literami A i B), w których syntezie bierze udział związek X.
reakcje substytucji, addycji i eliminacji
Arkusz diagnostyczny z chemii 2022 grudzień
Jedną z monobromopochodnych butanu (związek A) poddano reakcji z KOH w bezwodnym etanolu (reakcja 1.), a na otrzymany związek B podziałano bromowodorem (reakcja 2.). Główny produkt C był izomerem związku A.
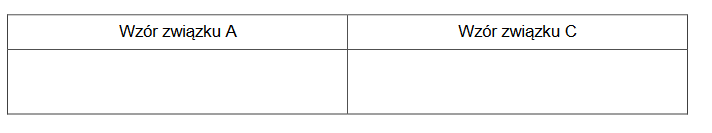
Uzupełnij poniższe zdanie. Wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. Następnie uzupełnij tabelę. Napisz wzory półstrukturalne (grupowe) związków A i C.
Związek B powstał w reakcji (substytucji / addycji / eliminacji), a jego przemiana w związek C jest przykładem reakcji (substytucji / addycji / eliminacji).
właściwości chemiczne fenoli w reakcji z wodorotlenkiem sodu
Arkusz diagnostyczny z chemii 2022 grudzień
W temperaturze powyżej 67°C fenol miesza się z wodą w dowolnych proporcjach, natomiast w przedziale temperatury 15–40°C jego maksymalne stężenie w roztworze wodnym nie przekracza 10 %.
Do probówki wprowadzono fenol i wodę w stosunku masowym 1 : 5 i przeprowadzono doświadczenie.
Etap 1. Zawartość probówki ogrzano do temperatury 70 °C.
Etap 2. Mieszaninę ochłodzono do temperatury 25 °C.
Etap 3. Dodano stechiometryczną ilość wodorotlenku sodu (w stosunku do fenolu).
1. Uzupełnij tabelę. Opisz wygląd zawartości probówki po kolejnych etapach doświadczenia.

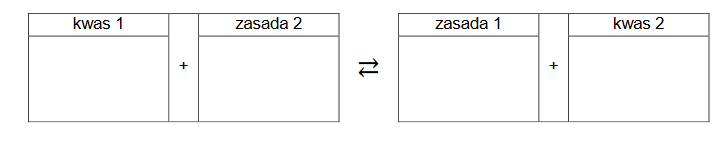
2. Po pewnym czasie stwierdzono, że mieszanina otrzymana w 3. etapie ma odczyn zasadowy.
Napisz równanie reakcji odpowiadającej za odczyn tej mieszaniny na podstawie definicji kwasów i zasad Brønsteda. Wzory odpowiednich drobin wpisz w poniższą tabelę.
właściwości chemiczne węglowodorów aromatycznych
Arkusz diagnostyczny z chemii 2022 grudzień
W wyniku działania kwasem azotowym(III) na pierwszorzędowe aminy aromatyczne powstają tzw. sole diazoniowe, które znajdują zastosowanie w syntezie organicznej.
W praktyce, zamiast nietrwałego kwasu azotowego(III) stosuje się jego sól w obecności mocnego kwasu. Przykład takiej reakcji z udziałem aniliny zilustrowano równaniem:
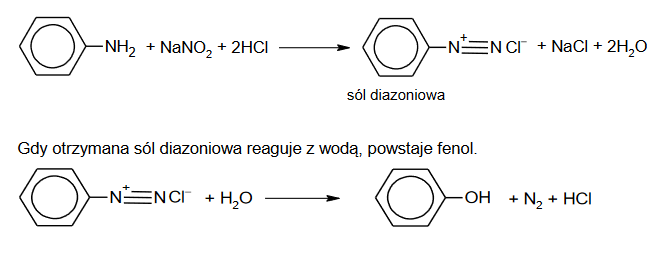
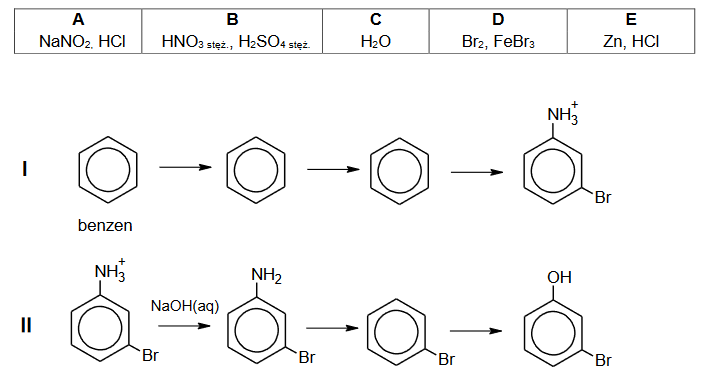
Opisane przemiany mogą być stosowane w celu otrzymania pochodnych benzenu, w których podstawniki kierujące w pozycje orto– i para– znajdują się względem siebie w pozycji meta–.
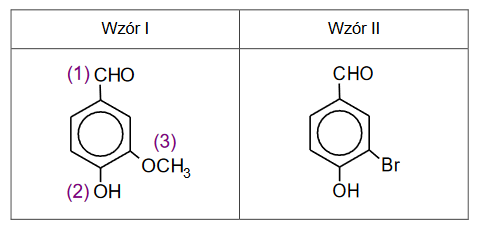
Zaprojektuj ciąg przemian, w wyniku których z benzenu powstanie 3–bromofenol – uzupełnij w poniższym, dwuczęściowym schemacie wzory produktów pośrednich, a nad każdą strzałką wpisz literę oznaczającą zestaw użytych reagentów. Zestawy odczynników wybierz spośród wymienionych poniżej.
odróżnianie alkoholi trzeciorzędowych od alkoholi pierwszo- i drugorzędowych
Arkusz diagnostyczny z chemii 2022 grudzień
Izomeryczne związki A, B i C należące do jednej klasy związków organicznych mają wzór sumaryczny C₄H₁₀O. Jeden z tych związków ma rozgałęziony łańcuch węglowy. Izomer A został wprowadzony do roztworu K₂Cr₂O₇ z dodatkiem kwasu siarkowego(VI) i na zdjęciu obok pokazano, jak wygląda zawartość probówki na początku tego doświadczenia (1) oraz po pewnym czasie (2).

Wiadomo, że cząsteczki związku A nie są chiralne, ale jego izomer B, który podobnie zachowałby się w opisanym doświadczeniu, wykazuje czynność optyczną. Izomer C nie ulega działaniu jonów dichromianowych(VI).
Napisz wzory półstrukturalne (grupowe) izomerów A, B, C.
aflatoksyna B1 – silnie toksyczny, rakotwórczy związek wytwarzany przez pleśnie
Arkusz diagnostyczny z chemii 2022 grudzień
Jednym z silnie toksycznych związków wytwarzanych przez pleśnie jest aflatoksyna B1, wykazująca właściwości rakotwórcze. Poniższy wzór przedstawia strukturę cząsteczki tego związku.
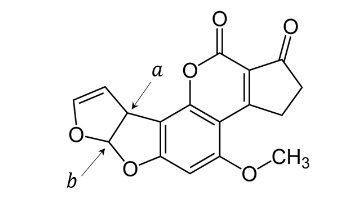
Uzupełnij tabelę. Wpisz formalne stopnie utlenienia atomów węgla oznaczonych literami 𝒂 i 𝒃 we wzorze cząsteczki aflatoksyny B1 oraz określ typ hybrydyzacji, jaki można przypisać orbitalom walencyjnym atomu węgla 𝒂.

tworzenie wzoru dipeptydów i tripeptydów
Arkusz diagnostyczny z chemii 2022 grudzień
Pewien tripeptyd zbudowany z aminokwasów białkowych zawiera w każdej ze swoich cząsteczek cztery atomy tlenu, cztery atomy azotu i dwa asymetryczne atomy węgla. Dwa aminokwasy wchodzące w skład tego tripeptydu mają 4–węglowe łańcuchy boczne. Reszty aminokwasów są uporządkowane zgodnie ze wzrostem ich mas cząsteczkowych, czyli największą masę cząsteczkową ma aminokwas z wolną grupą karboksylową.
Napisz wzór tripeptydu spełniającego opisane warunki. Użyj trzyliterowych kodów aminokwasów. Pamiętaj, że z lewej strony umieszcza się kod aminokwasu, którego reszta zawiera wolną grupę aminową połączoną z atomem węgla α.