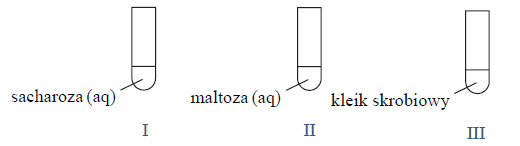Ustalanie liczby oktanowej.
Arkusz maturalny z chemii rozszerzonej czerwiec 2017 stara formuła
W celu ustalenia liczby oktanowej LO benzyny porównuje się proces spalania badanego paliwa ze spalaniem mieszanki wzorcowej złożonej z dwóch składników: n-heptanu i 2,2,4-trimetylopentanu.
1. Napisz wzór półstrukturalny (grupowy) 2,2,4-trimetylopentanu oraz oceń, czy ten związek jest izomerem n-heptanu. Ocenę uzasadnij.
2. Napisz, czy cząsteczki 2,2,4-trimetylopentanu są chiralne. Odpowiedź uzasadnij.
Zadanie 34.
2017 czerwiec SR
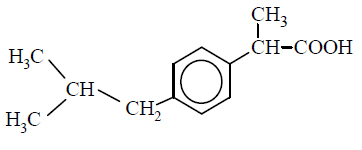
W poniższym wzorze ilustrującym budowę cząsteczki ibuprofenu podkreśl symbol asymetrycznego atomu węgla.
Polimery PGA i PLA.
Arkusz maturalny z chemii rozszerzonej czerwiec 2017 stara formuła
Poniżej przedstawiono wzory PGA i PLA, popularnych polimerów, które w pełni ulegają biodegradacji.
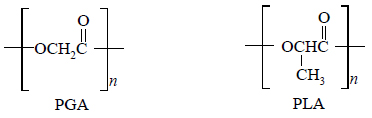
1. Podaj nazwę klasy tworzyw sztucznych, do których zakwalifikujesz PGA i PLA.
2. Podaj wzór półstrukturalny (grupowy) monomeru PGA i nazwę monomeru PLA.