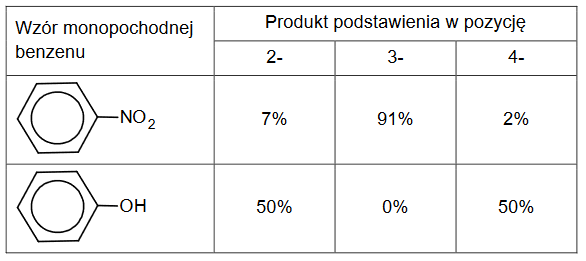
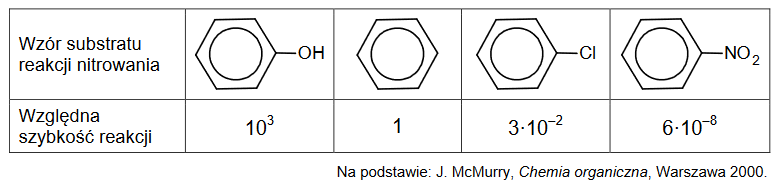
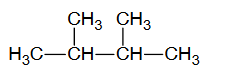reakcja nitrowania węglowodorów
INFORMATOR o egzaminie maturalnym z chemii 22/23
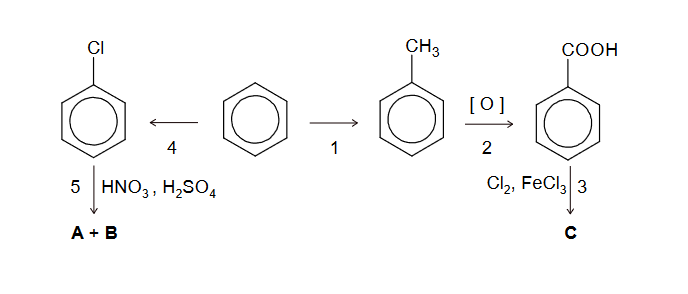
Dwa węglowodory aromatyczne – A i B – mają wzór sumaryczny C₈H₁₀. Izomer A w wyniku reakcji nitrowania tworzy wyłącznie jedną mononitropochodną. Izomer B poddany reakcji monochlorowania w obecności światła, a następnie – reakcji z wodnym roztworem KOH, tworzy alkohol drugorzędowy.
1. Napisz równanie reakcji mononitrowania związku A – zastosuj wzory półstrukturalne (grupowe) lub uproszczone związków organicznych. Podaj nazwę systematyczną produktu mononitrowania związku A.
Równanie reakcji:
Nazwa systematyczna produktu mononitrowania związku A:
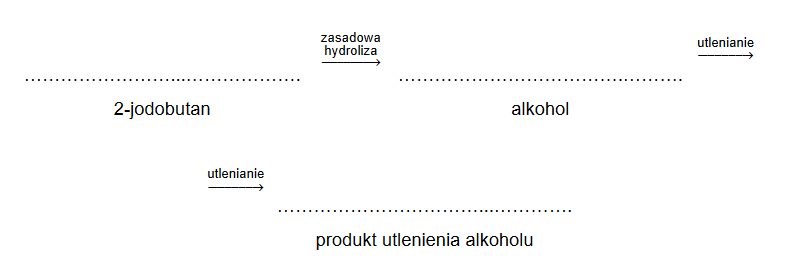
2. Uzupełnij schemat ciągu przemian prowadzonych od związku B do alkoholu. Związki organiczne przedstaw za pomocą wzorów półstrukturalnych (grupowych) albo uproszczonych.

półstrukturalne wzory węglowodorów
Arkusz z chemii rozszerzonej czerwiec 2021
O dwóch alkanach A i B wiadomo, że:
• cząsteczki każdego alkanu zbudowane są z pięciu atomów węgla
• alkan A tworzy w reakcji z bromem wyłącznie jedną monobromopochodną
• w cząsteczce alkanu B jest jeden atom węgla na –I stopniu utlenienia.
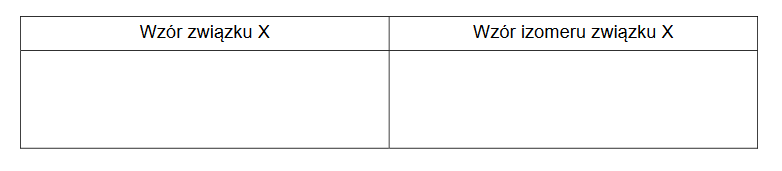
Uzupełnij tabelę. Narysuj wzór półstrukturalny (grupowy) monobromopochodnej alkanu A i wzór półstrukturalny (grupowy) alkanu B oraz napisz nazwy systematyczne obu związków.

elementarny wzór związku organicznego
Arkusz z chemii rozszerzonej czerwiec 2021
W wyniku spalenia 1,00 g związku organicznego w nadmiarze tlenu uzyskano jako jedyne produkty: 1,42 g CO₂ oraz 0,87 g H₂O.
Wykonaj odpowiednie obliczenia i napisz elementarny (najprostszy) wzór związku organicznego, który spalono.
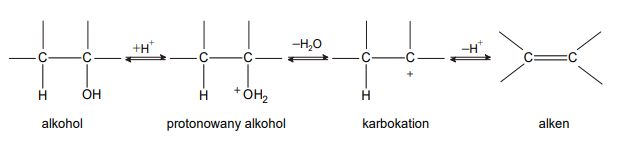
otrzymywanie alkenów poprzez reakcję eliminacji wody z alkoholi
Arkusz z chemii rozszerzonej maj 2021
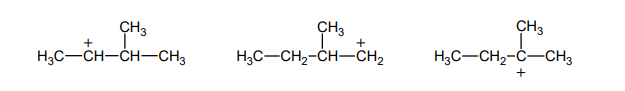
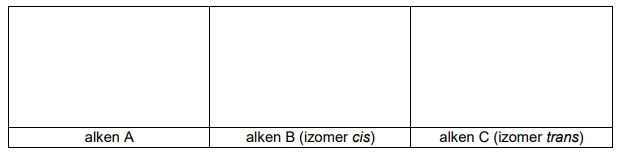
Alkeny można otrzymać m.in. w wyniku reakcji eliminacji wody z alkoholi (tzw. reakcja dehydratacji alkoholi). Poddano dehydratacji 3-metylobutan-2-ol i otrzymano mieszaninę alkenów A i B, przy czym alken A jest produktem głównym (atom wodoru jest odrywany w tym przypadku od tego atomu węgla, który jest połączony z mniejszą liczbą atomów wodoru), a alken B – produktem ubocznym przemiany.
1. Produkt A można także otrzymać w wyniku dehydratacji innego alkoholu.
Podaj wzór półstrukturalny (grupowy) i nazwę systematyczną tego alkoholu.
Wzór:
Nazwa systematyczna:
2. Napisz równanie reakcji alkenu A z bromowodorem (HBr) prowadzącej do powstania produktu głównego tej przemiany. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
węglowodory pierścieniowe
Arkusz z chemii rozszerzonej maj 2021
Poniżej przedstawiono wzory dwóch związków organicznych: mentolu i tymolu.
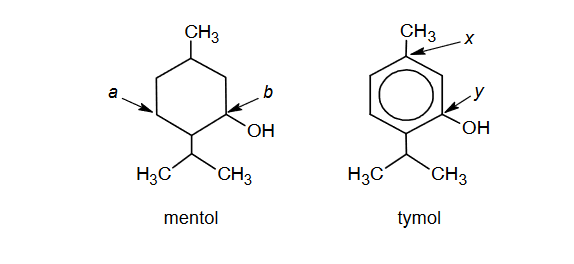
1. Uzupełnij poniższe tabele.
• Określ hybrydyzację orbitali walencyjnych: atomu węgla oznaczonego we wzorze mentolu literą a oraz atomu węgla oznaczonego we wzorze tymolu literą x.

• Określ formalne stopnie utlenienia: atomu węgla oznaczonego we wzorze mentolu literą b oraz atomu węgla oznaczonego we wzorze tymolu literą y.
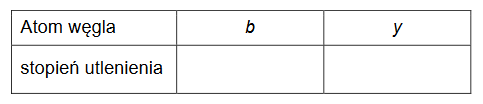
2. Rozstrzygnij, czy cząsteczka tymolu jest chiralna. Odpowiedź uzasadnij.
Rozstrzygnięcie:
Uzasadnienie:
ciąg przemian chemicznych
Arkusz z chemii rozszerzonej marzec 2021
Poniżej przedstawiono ciąg przemian chemicznych, w których biorą udział związki organiczne, umownie oznaczone literami A, B, C i D, a produktem ostatecznym jest 2-bromopropan. Związek B jest izomerem, w którym atom chloru jest przyłączony do atomu węgla o niższej rzędowości.
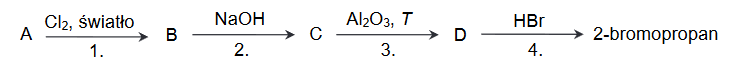
1. Napisz równania reakcji oznaczonych numerami 1 i 3. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
Reakcja 1.:
Reakcja 3.:
2. Uzupełnij poniższą tabelę. Określ typ reakcji 2. (addycja, eliminacja, substytucja) oraz jej mechanizm (rodnikowy, elektrofilowy, nukleofilowy).

budowa enancjomerów cysteiny
Arkusz z chemii rozszerzonej marzec 2021
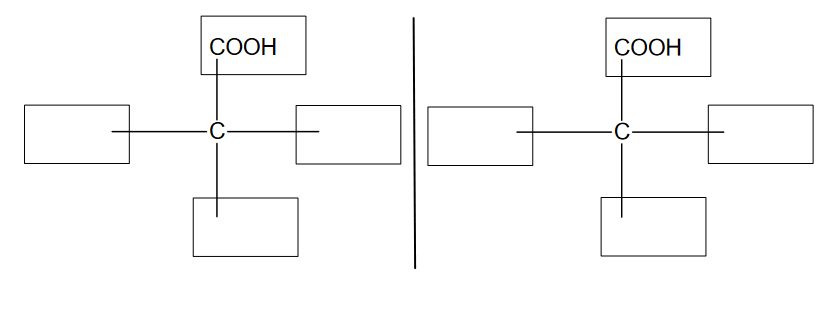
Uzupełnij poniższy schemat tak, aby przedstawiał budowę obu enancjomerów cysteiny.
energia potencjalna cząsteczek metanu
Arkusz maturalny z chemii rozszerzonej lipiec 2020 Formuła 2015
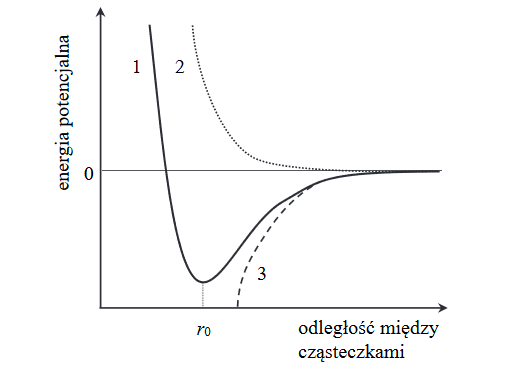
Na poniższym wykresie przedstawiono, jak zmienia się energia potencjalna cząsteczek metanu w zależności od dzielącej je odległości (linia ciągła oznaczona numerem 1).
Uzupełnij poniższe zdania. Wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie.
W miarę zbliżania się do siebie cząsteczek metanu siły przyciągania van der Waalsa rosną, co skutkuje spadkiem energii potencjalnej cząsteczek zilustrowanym krzywą oznaczoną numerem (2 / 3). Jednocześnie w miarę zbliżania się do siebie cząsteczek metanu siły odpychania między jądrami atomowymi i siły odpychania między elektronami dwóch cząsteczek (rosną / maleją). Najbardziej korzystny energetycznie dla cząsteczek metanu jest stan, w którym odległość między nimi jest (mniejsza niż r0 / równa r0 / większa od r0 ).