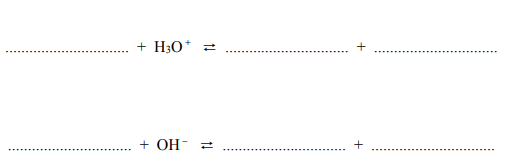Równania procesu redukcji i procesu utleniania. Siarczan (VI) manganu (II), siarczan (IV) potasu.
Arkusz maturalny z chemii rozszerzonej 2018 nowa formuła
Przeprowadzono doświadczenie, którego przebieg zilustrowano na schemacie.
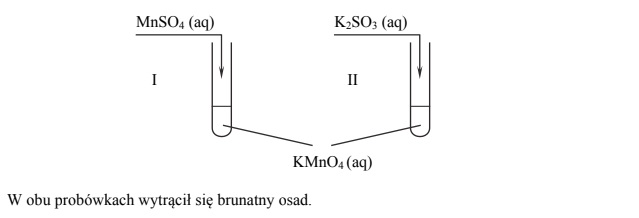
Napisz w formie jonowej z uwzględnieniem oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równania procesu redukcji i procesu utleniania zachodzących w probówce I podczas opisanego doświadczenia. Uwzględnij fakt, że jednym z substratów obu procesów jest woda.
Równanie procesu redukcji:
Równanie procesu utleniania:
Oceń, jaki jest odczyn roztworu po zakończeniu reakcji w probówce I, oraz podaj nazwę anionu zawierającego siarkę, który powstał w wyniku reakcji chemicznej przebiegającej w probówce II.
Odczyn roztworu po reakcji w probówce I:
Nazwa anionu zawierającego siarkę:
Wodny roztwór etanianu magnezu i etanianu sodu.
Arkusz maturalny z chemii rozszerzonej 2018 nowa formuła

W dwóch nieopisanych probówkach znajdują się wodne roztwory dwóch soli (każdy roztwór w innej probówce). Wiadomo, że jednym roztworem jest wodny roztwór etanianu (octanu) magnezu, a drugim – wodny roztwór etanianu (octanu) sodu.
Oceń, czy po dodaniu wodnego roztworu kwasu ortofosforowego(V) do obu probówek i ogrzaniu ich zawartości możliwe będzie wskazanie, w której probówce znajdował się wodny roztwór etanianu magnezu, a w której – wodny roztwór etanianu sodu. Odpowiedź uzasadnij.
Stałe dysocjacji kwasów organicznych i nieorganicznych.
Arkusz maturalny z chemii rozszerzonej 2018 maj stara formuła
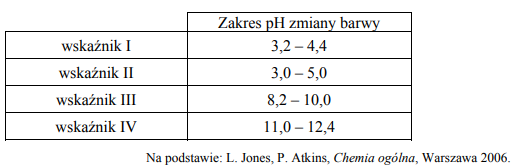
W poniższej tabeli podane są wartości stałej dysocjacji wybranych związków w temperaturze T.
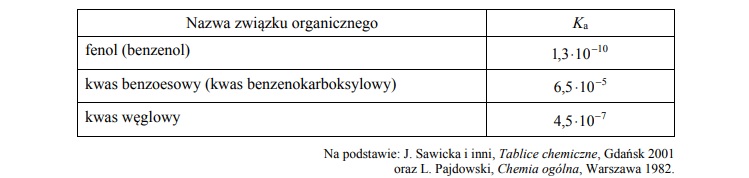
W dwóch nieoznakowanych probówkach znajdują się oddzielnie wodne roztwory kwasu
benzoesowego i fenolu.
Wyjaśnij, dlaczego możliwe jest odróżnienie wodnego roztworu kwasu benzoesowego
od wodnego roztworu fenolu przy użyciu stałego Na2CO3.
Napisz w formie cząsteczkowej równanie reakcji, która jest podstawą eksperymentu.
Barwy jonów chromu i żelaza
Arkusz maturalny z chemii rozszerzonej maj 2018 nowa formuła
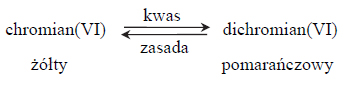
Przeprowadzono doświadczenia, których przebieg zilustrowano na schemacie:
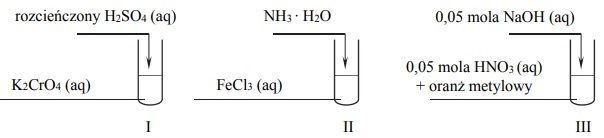
Oceń, czy poniższe informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.

Porówanie charakteru kwasowego fenolu, kwasu węglowego i kwasu chlorowodorowego
Arkusz maturalny z chemii rozszerzonej maj 2018 nowa formuła
Za pomocą odpowiednio przeprowadzonych doświadczeń można porównać charakter kwasowy fenolu, kwasu solnego i kwasu węglowego.
Zaprojektuj jedno doświadczenie, którym potwierdzisz, że spośród wymienionych substancji najmocniejszym kwasem jest kwas solny, a najsłabszym – fenol. W tym celu uzupełnij schemat doświadczenia. Wpisz wzory wszystkich związków, których wodnych roztworów należy użyć w doświadczeniu. Substancje wybierz spośród następujących:
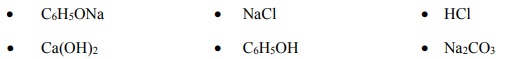
Wszystkie roztwory były świeżo przygotowane.
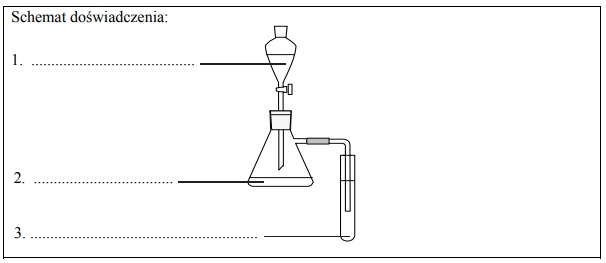
Napisz, co będzie można zaobserwować podczas przeprowadzonego doświadczenia.
Kolba:
Probówka:
Napisz w formie jonowej skróconej równania reakcji zachodzących w kolbie i w probówce podczas przeprowadzonego doświadczenia.
Równanie reakcji zachodzącej w kolbie:
Równanie reakcji zachodzącej w probówce:
Uszereguj wodne roztwory elektrolitów zgodnie z pH
Arkusz maturalny z chemii rozszerzonej maj 2018 nowa formuła
W temperaturze T przygotowano wodne roztwory pięciu elektrolitów o jednakowym stężeniu molowym równym 0,1 3 mol dm− ⋅ . Poniżej podano wzory tych elektrolitów.
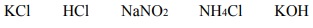
Uszereguj związki o podanych wzorach zgodnie z rosnącym pH ich wodnych roztworów. Napisz wzory tych związków w odpowiedniej kolejności.

Miareczkowanie kwasu octowego roztworem zasady sodowej.
Arkusz maturalny z chemii rozszerzonej maj 2018 nowa formuła
Do wodnego roztworu kwasu etanowego (octowego) o określonej objętości, ale o nieznanym stężeniu, dodawano kroplami wodny roztwór wodorotlenku sodu o znanym stężeniu i za pomocą pehametru mierzono pH mieszaniny reakcyjnej. W ten sposób przeprowadzono tzw. miareczkowanie pehametryczne, które jest jedną z metod analizy ilościowej. W czasie doświadczenia zachodziła reakcja opisana równaniem:
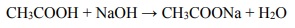
Zestaw użyty w tym doświadczeniu przedstawiono na poniższym schemacie, a otrzymane wyniki miareczkowania umieszczono na wykresie.
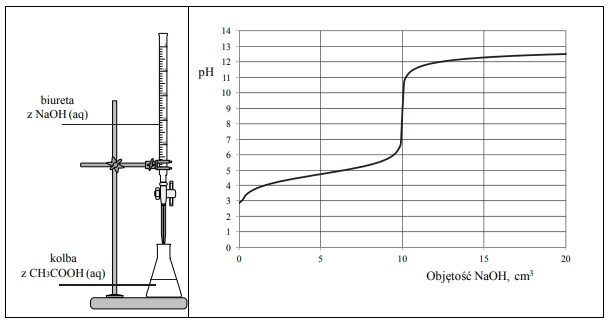
Po dodaniu takiej objętości roztworu wodorotlenku sodu, w jakiej znajdowała się liczba moli NaOH równa liczbie moli CH3COOH w roztworze wziętym do analizy, w układzie został osiągnięty punkt równoważnikowy. Ustalono, że w opisanym doświadczeniu pH w punkcie równoważnikowym było równe 9.
Podaj wzór jonu, którego stężenie jest największe w roztworze otrzymanym po dodaniu 18 cm3 wodnego roztworu wodorotlenku sodu do analizowanego roztworu kwasu etanowego.
Hydrat tiosiarczanu sodu.
Arkusz maturalny z chemii rozszerzonej czerwiec 2017 nowa formuła
W wyniku reakcji chemicznej roztworu siarczanu(IV) sodu z siarką otrzymuje się wodny roztwór tiosiarczanu sodu. Proces ten można opisać równaniem:
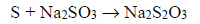
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004.
W wodzie rozpuszczono 6,3 g
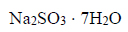
i dodano nadmiar siarki. Otrzymaną mieszaninę gotowano przez pewien czas, po czym przesączono w celu usunięcia nadmiaru siarki. Z przesączu po ochłodzeniu otrzymano 5,2 g kryształów uwodnionego tiosiarczanu sodu. Ten związek, poddany odwodnieniu pod obniżonym ciśnieniem, zmniejszył swoją masę o 36,3%
Wykonaj odpowiednie obliczenia i podaj wzór hydratu tiosiarczanu sodu, który otrzymano z mieszaniny poreakcyjnej w wyniku krystalizacji.