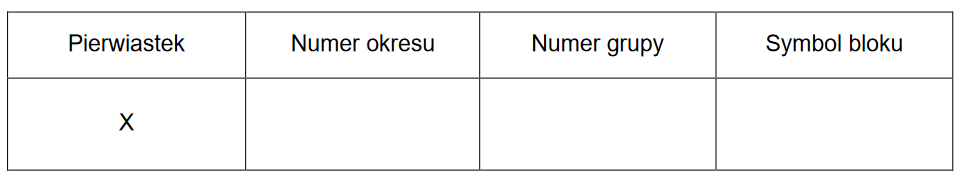
Liczba koordynacyjna
Arkusz z chemii rozszerzonej maj 2024 Formuła 2015
Liczba koordynacyjna to liczba najbliższych atomów lub jonów otaczających dany atom lub jon w sieci krystalicznej kryształu.
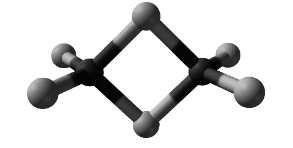
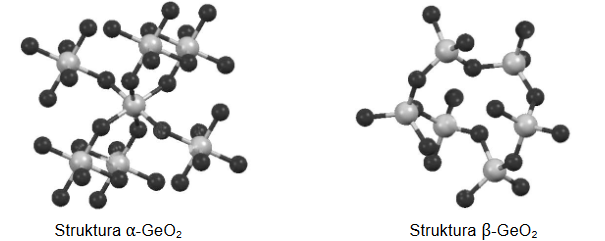
Tlenek germanu(IV) jest krystalicznym ciałem stałym. Istnieje w dwóch odmianach: alfa, α-GeO2, oraz beta, β-GeO2. Fragmenty struktur obu odmian przedstawiono poniżej (atomy Ge – szare, atomy O – czarne).
Uzupełnij zdania. Wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie.
W odmianie α-GeO2 liczba koordynacyjna dla atomu germanu wynosi (dwa / cztery / sześć). W strukturze odmiany β-GeO2 dla orbitali walencyjnych atomu germanu zakłada się hybrydyzację (sp2 / sp3).
definicja kwasu i zasady Brønsteda
Arkusz z chemii rozszerzonej maj 2024 Formuła 2023
Przeprowadzono reakcje zgodnie ze schematem:
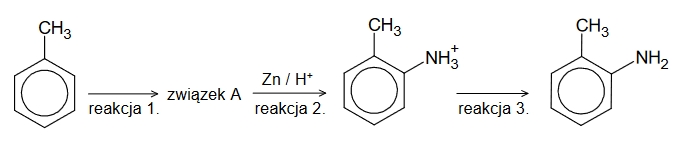
1. Wpisz do schematu wzory odpowiednich drobin, tak aby powstało równanie reakcji 3. w formie jonowej skróconej. Zastosuj definicję kwasu i zasady Brønsteda.
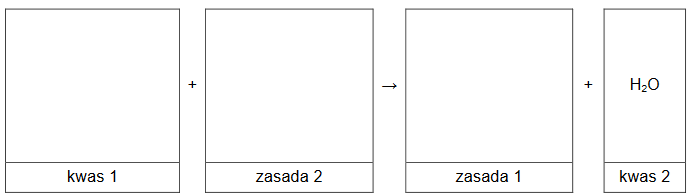
2. Organiczny związek otrzymany w reakcji 3. zmieszano z bromem (w stosunku molowym 1 : 1) i poddano reakcji w obecności światła.
Narysuj wzór półstrukturalny lub uproszczony organicznego produktu opisanej reakcji i uzupełnij zdanie. Wybierz i zaznacz właściwą odpowiedź spośród podanych w nawiasie.
Opisana przemiana (jest / nie jest) reakcją utlenienia-redukcji.
hydroliza wodnego roztworu tetraoksokrzemianu(IV) sodu
Arkusz z chemii rozszerzonej czerwiec 2023 nowa formuła
Stapianie tlenku krzemu(IV) z wodorotlenkiem sodu pozwala otrzymać różne krzemiany, w zależności od stosunku molowego substratów tej reakcji. Wskutek hydrolizy wodnego roztworu tetraoksokrzemianu(IV) sodu, czyli Na4SiO4, tworzy się roztwór silnie alkaliczny. Taki roztwór obok cząsteczek kwasu tetraoksokrzemowego(IV) zawiera wszystkie rodzaje wodoroanionów tego kwasu.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010
1. Napisz w formie cząsteczkowej równanie reakcji otrzymywania tetraoksokrzemianu(IV) sodu opisaną metodą. Oblicz stosunek masowy substratów.
Równanie reakcji:
Stosunek masowy:
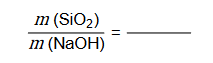
2. Napisz wzór sumaryczny tego wodoroanionu kwasu tetraoksokrzemowego(IV), który zbudowany jest z siedmiu atomów.
3. Narysuj elektronowy wzór kreskowy kwasu tetraoksokrzemowego(IV). Określ typ hybrydyzacji (sp, sp2, sp3) orbitali walencyjnych atomu krzemu w cząsteczce tego kwasu.
Elektronowy wzór kreskowy:
Typ hybrydyzacji:
zasady rozmieszczania elektronów na orbitalach
Arkusz diagnostyczny z chemii 2022 grudzień
Na zdjęciu obok przedstawiono wodny roztwór soli, w skład której wchodzą pierwiastki X1, X2 i X3. Dwa z nich są w stanie wolnym metalami i należą do tego samego okresu, a jeden jest niemetalem i leży w innym okresie. Masy atomowe tych trzech pierwiastków, zaokrąglone do liczb całkowitych, spełniają zależność: M X1 + M X2 = M X3. Atom pierwiastka X3 ma na zewnętrznej powłoce dwa razy więcej elektronów niż atom pierwiastka X2, a atom pierwiastka X1 ma na zewnętrznej powłoce dwa razy więcej niesparowanych elektronów niż atom pierwiastka X2.

1. Zidentyfikuj pierwiastki X1, X2 oraz X3. Napisz ich symbole chemiczne.
X1:
X2:
X3:
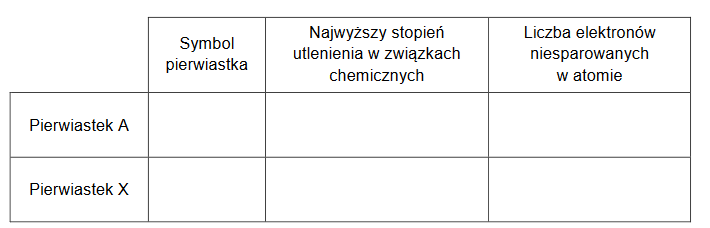
2. Uzupełnij poniższą tabelę. Wpisz wartości liczb kwantowych odpowiadających niesparowanym elektronom w atomach (w stanie podstawowym) pierwiastków X1 i X3.

typowe właściwości chemiczne tlenków pierwiastków
Arkusz diagnostyczny z chemii 2022 grudzień
W trzech probówkach oznaczonych numerami 1, 2, 3, znajdowała się woda z dodatkiem oranżu metylowego. Do każdej z tych probówek wprowadzono małą porcję jednego z tlenków wybranych z poniższego zbioru:
Na₂O
SiO₂
P₄O₁₀
CuO
Zawartość każdej z probówek wymieszano i pozostawiono na pewien czas.

1. Uzupełnij tabelę. Wpisz wzory tlenków wprowadzonych do probówek 1 i 2.

2. Napisz w formie cząsteczkowej równanie reakcji, której produkt spowodował zmianę barwy oranżu metylowego w probówce 3.
Budowa atomu
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Na podstawie budowy atomów pierwiastków należących do grup 1.–2. oraz 13.–17. drugiego okresu układu okresowego uzupełnij poniższe zdanie. W wyznaczone miejsca wpisz symbol albo nazwę odpowiedniego pierwiastka.
Spośród pierwiastków drugiego okresu:
• najmniejszy ładunek jądra ma atom:
• najmniejszy promień atomowy ma atom:
• najmniejszą wartość pierwszej energii jonizacji ma atom:
świeżo strącony wodorotlenek miedzi(II) z biuretem – efekty doświadczenia
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Przeprowadzono doświadczenie polegające na dodaniu świeżo strąconego wodorotlenku miedzi(II) do probówki zawierającej wodny roztwór biuretu H2N–CO–NH–CO–NH2.
Spośród poniższych ilustracji wybierz i zaznacz tę, która przedstawia efekt opisanego doświadczenia.