Równanie kinetyczne reakcji – obliczenia
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Wróć do listyRównanie kinetyczne reakcji opisanej równaniem:
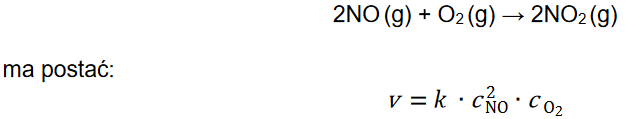
Szybkość reakcji chemicznej v, wyrażona w jednostce: mol *dm−3 * s−1, zależy od stężeń molowych substratów reakcji oraz od stałej szybkości reakcji 𝑘 – współczynnika charakterystycznego dla danej reakcji. Stała szybkości reakcji zależy od temperatury, a nie zależy od stężenia substratów.
1. Napisz jednostkę stałej szybkości reakcji 𝒌 w równaniu kinetycznym opisanej reakcji.
2. W zamkniętym reaktorze o pojemności 2 dm3 zmieszano 6 moli tlenku azotu(II) i 4 mole tlenu. Podczas reakcji utrzymywano stałą temperaturę T.
Oblicz, ile razy zmaleje szybkość opisanej reakcji w stosunku do szybkości
początkowej, w momencie, w którym stężenie tlenu zmniejszy się o 1 mol * dm−3.

KOREPETYCJE