Kinetyka i statyka chemiczna
Arkusz z chemii rozszerzonej czerwiec 2021
Wróć do listyDo reaktora, w którym znajdowała się stała substancja X, wprowadzono pod ciśnieniem atmosferycznym gazową substancję Y i zapoczątkowano reakcję chemiczną, w wyniku której powstawał gaz Z. Po 10 minutach, w temperaturze T1, ustaliła się równowaga opisana równaniem:
X (s) + Y (g) ⇄ Z (g)
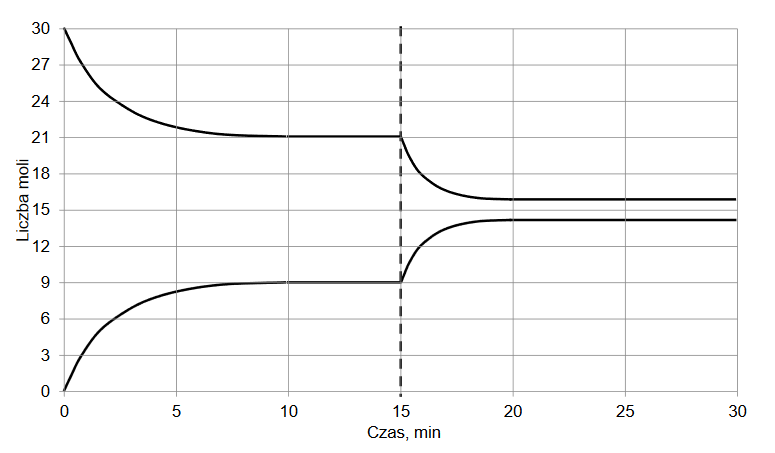
Na wykresie przedstawiono wyniki pomiaru liczby moli gazowych reagentów w trakcie trwania procesu oraz po ustaleniu się stanu równowagi w temperaturze T1. W piętnastej minucie
eksperymentu zmieniono w układzie temperaturę na T2 wyższą od T1, czego konsekwencją było ustalenie się nowego stanu równowagi po dwudziestu minutach eksperymentu, co także
zilustrowano na poniższym wykresie.
1. Rozstrzygnij, czy w temperaturze T2 – w porównaniu z przemianą zachodzącą w temperaturze T1 – następuje:
• wzrost szybkości reakcji tworzenia substancji Z;
• spadek szybkości reakcji rozkładu substancji Z.
Odpowiedzi uzasadnij.
2. Rozstrzygnij, czy reakcja tworzenia związku Z jest procesem endoenergetycznym. Odpowiedź uzasadnij.
Rozstrzygnięcie:
Uzasadnienie:
3. Napisz wyrażenie na stężeniową stałą równowagi reakcji tworzenia związku Z i oszacuj jej wartość w temperaturze T1. Uwzględnij fakt, że w wyrażeniu na stałą równowagi tej reakcji pomija się stężenie substancji stałej.
Wyrażenie na stałą równowagi:
Oszacowana wartość stałej równowagi:
4. Uzupełnij poniższe zdanie. Wybierz i zaznacz jedną odpowiedź spośród podanych w nawiasie.
Wraz ze zmniejszeniem ciśnienia w układzie w warunkach izotermicznych wydajność reakcji otrzymywania substancji Z (wzrośnie / zmaleje / się nie zmieni).

KOREPETYCJE