Reakcja estryfikacji w środowisku kwasowym
Arkusz z chemii rozszerzonej maj 2021
Wróć do listyReakcja estryfikacji, w której uczestniczą kwas etanowy i butan-2-ol, zachodzi w środowisku kwasowym zgodnie z równaniem:
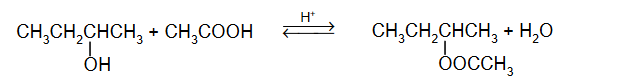
W temperaturze T stężeniowa stała równowagi tej reakcji Kc = 2,12.
1. Oblicz, ile gramów bezwodnego kwasu etanowego należy użyć do reakcji z jednym molem butan-2-olu w temperaturze T, aby przereagowało 85% początkowej ilości butan-2-olu.
2. Uzupełnij poniższe zdania. Wybierz i podkreśl jedną odpowiedź spośród podanych w każdym nawiasie.
Przy użyciu w opisanej reakcji równomolowej mieszaniny kwasu i alkoholu wydajność tej reakcji jest w temperaturze T (niższa niż / równa / wyższa od) 85%. Opisaną reakcję przeprowadza się w środowisku kwasowym, ponieważ jony H + (katalizują tę reakcję / zwiększają wydajność tej reakcji). W środowisku zasadowym opisany ester ulega hydrolizie, której produktami są butan-2-ol
i (kwas etanowy / sól kwasu etanowego).

KOREPETYCJE